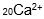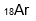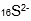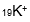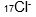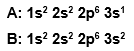|
1 |
Salah satu peran ilmu kimia yaitu dalam bidang industri farmasi. Ilmu kimia menjadi landasan fundamental dalam upaya penemuan dan pengembangan obat-obatan baru untuk mengatasi berbagai penyakit, dari infeksi sederhana hingga penyakit kompleks seperti kanker dan gangguan genetik. Proses pengembangan obat modern dimulai dari pemahaman mendalam tentang bagaimana molekul obat berinteraksi dengan target biologis dalam tubuh, seperti protein atau DNA. Ilmu kimia yang harus dipelajari oleh para peneliti sehingga memungkinkan para peneliti untuk merancang (sintesis) molekul-molekul obat potensial dengan struktur tertentu yang dapat mengikat target biologis secara efektif adalah… |
|
|
A |
Kimia Analisis |
|
|
B |
Kimia fisika |
|
|
C |
Kimia Organik |
|
|
D |
Kimia Anorganik |
|
|
E |
Kimia lingkungan |
|
|
2 |
Besi adalah logam yang berasal dari bijih besi (tambang) yang banyak digunakan dalam kehidupan manusia sehari-hari. Dalam tabel periodik, besi mempunyai simbol Fe dengan nomor atom 26 dan nomor massa 56. Besi murni berwarna abu-abu keperakan, bersifat liat, dan dapat ditempa. Salah satu sifat besi adalah kemampuannya sebagai konduktor panas dan listrik yang baik. Selain itu, besi memiliki titik lebur yang tinggi (sekitar 1.535°C untuk besi murni) dan bersifat magnetis, yang memungkinkannya ditarik oleh magnet. Namun, besi memiliki kelemahan signifikan, yaitu mudah mengalami korosi (berkarat). Berdasarkan wacana di atas, yang merupakan sifat fisika besi adalah…
|
|
|
A |
Jika 1, 2, dan 3 benar |
|
|
B |
jika 1 dan 3 benar |
|
|
C |
jika 2 dan 4 benar |
|
|
D |
jika hanya 4 yang benar |
|
|
E |
jika 1, 2, 3, dan 4 benar |
|
|
3 |
Perhatikan sifat zat berikut!
Yang merupakan sifat campuran homogen adalah… |
|
|
A |
(1), (2), dan (5) |
|
|
B |
(1), (2), dan (3) |
|
|
C |
(1), (3), dan (4) |
|
|
D |
(2), (3), dan (4) |
|
|
E |
(3), (4), dan (5) |
|
|
4 |
Udara yang kita hirup setiap saat adalah sebuah campuran gas yang kompleks dan vital untuk menopang kehidupan di Bumi. Unsur gas yang paling melimpah di udara adalah nitrogen (N₂), yang menyusun sekitar 78% dari total volume udara. Unsur terpenting kedua adalah oksigen (O₂), yang mengisi sekitar 21% dari atmosfer. Sisanya, sekitar 1%, terdiri dari berbagai gas lain, yang meliputi argon (Ar) sekitar 0,93%, karbon dioksida (CO₂) sekitar 0,04%, serta gas-gas jejak lainnya seperti neon (Ne), helium (He), metana (CH4), dan kripton (Kr). Berdasarkan wacana di atas, yang termasuk molekul unsur adalah… |
|
|
A |
Ar, Ne, He, dan Kr |
|
|
B |
N₂, O₂, CO₂ dan CH4 |
|
|
C |
N₂ dan O₂ |
|
|
D |
CO₂ dan CH4 |
|
|
E |
Ar, Ne, He, Kr, N₂ dan O₂ |
|
|
5 |
Perhatikan beberapa kejadian berikut :
Kejadian yang tergolong perubahan kimia adalah… |
|
|
A |
1, 3, dan 5 |
|
|
B |
2, 3, dan 4 |
|
|
C |
2, 4, dan 5 |
|
|
D |
3, 4, dan 5 |
|
|
E |
2, 3, dan 5 |
|
|
Soda kue mempunyai rumus kimia NaHCO3 adalah bahan pengembang kimia yang digunakan dalam pembuatan kue dan produk roti lainnya. Soda kue bisa mengembangkan adonan karena reaksi kimia yang terjadi ketika bahan ini bercampur dengan bahan asam seperti buttermilk dan dipanaskan. Ketika soda kue bereaksi dengan bahan asam dalam adonan kue, maka akan menghasilkan gas karbon dioksida, CO2. Saat adonan dipanaskan di dalam oven, gas karbon dioksida ini mengembang, menyebabkan adonan mengembang dan menjadi ringan dan berpori. Adonan yang mengembang dengan baik akan menghasilkan kue yang ringan dan bertekstur lembut. Berdasarkan teks di atas maka ciri reaksi kimia saat penggunaan soda kue adalah… |
||
|
A |
Perubahan suhu dan perubahan massa |
|
|
B |
Perubahan warna dan terbentuk endapan |
|
|
C |
Terbentuk gas dan perubahan massa |
|
|
D |
Perubahan suhu dan terbentuk endapan |
|
|
E |
Perubahan suhu dan terbentuk gas. |
|
|
Seorang siswa akan melakukan titrasi asam-basa untuk menentukan konsentrasi larutan
|
||
|
A |
Jika 1, 2, dan 3 benar |
|
|
B |
jika 1 dan 3 benar |
|
|
C |
jika 2 dan 4 benar |
|
|
D |
jika hanya 4 yang benar |
|
|
E |
jika 1, 2, 3, dan 4 benar |
|
|
Pernyataan Niels Bohr berikut tentang atom yang benar adalah…
|
||
|
A |
Jika 1, 2, dan 3 benar |
|
|
B |
jika 1 dan 3 benar |
|
|
C |
jika 2 dan 4 benar |
|
|
D |
jika hanya 4 yang benar |
|
|
E |
jika 1, 2, 3, dan 4 benar |
|
|
Perhatikan notasi unsur berikut
Jumlah proton, elektron, dan neutron dari unsur di atas adalah… |
||
|
A |
30; 30; 65 |
|
|
B |
65; 30; 30 |
|
|
C |
30; 30; 35 |
|
|
D |
30; 35; 30 |
|
|
E |
30; 35; 65 |
|
|
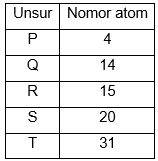
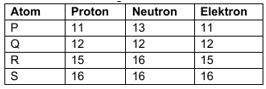
perhatikan data berikut:
Unsur yang merupakan pasangan isobar adalah… |
||
|
A |
P dan Q |
|
|
B |
P dan R |
|
|
C |
Q dan R |
|
|
D |
Q dan S |
|
|
E |
R dan S |
|
|
Menurut model atom Niels Bohr, elektron-elektron mengelilingi inti pada lintasan-lintasan tertentu yang disebut dengan kulit elektron atau tingkat energi. Elektron-elektron akan mulai menempati kulit pertama; K sampai penuh, kemudian mengisi kulit kedua; L dan demikian seterusnya. Jika suatu unsur mempunyai nomor atom 54, maka konfigurasi elektron menurut teori atom Bohr untuk unsur tersebut adalah… |
||
|
A |
2; 8; 8; 18; 18 |
|
|
B |
2; 8; 18; 18; 8 |
|
|
C |
2; 8; 18; 26 |
|
|
D |
2; 8; 18; 18; 2; 6 |
|
|
E |
2; 8; 18; 8; 18 |
|
|
Konfigurasi elektron mekanika kuantum adalah susunan elektron dalam atom yang didasarkan pada model atom mekanika kuantum, yang menjelaskan bahwa elektron berada dalam kulit, subkulit, dan orbital dengan tingkat energi tertentu, bukan pada orbit yang pasti seperti model atom Niels Bohr. Konfigurasi elektron menurut teori atom mekanika kuantum untuk unsur Mo dengan nomor atom 42 yang tepat adalah… |
||
|
A |
|
|
|
B |
|
|
|
C |
|
|
|
D |
|
|
|
E |
|
|
|
Salah satu cara atom mencapai kestabilan yaitu dengan melepaskan atau menerima elektron disebut pembentukan ion. Kestabilan ini terjadi ketika elektron terluar mencapai aturan oktet (delapan elektron valensi) atau duet (dua elektron valensi, khusus untuk hidrogen dan helium). Apabila atom galium; Ga yang memiliki massa atom 70 dan nomor atom 31 mencapai kestabilan dengan cara membentuk ion |
||
|
A |
|
|
|
B |
|
|
|
C |
|
|
|
D |
|
|
|
E |
|
|
|
Pada teori mekanika kuantum, terdapat empat bilangan kuantum yaitu bilangan kuantum utama (n), bilangan kuantum azimuth (l), bilangan kuantum magnetic (m) dan bilangan kuantum spin (s). Bilangan kuantum menyatakan kedudukan elektron dalam suatu atom dan membedakan dari elektron yang lain. Deret bilangan-bilangan kuantum yang mungkin bagi elektron 3d adalah… |
||
|
A |
n = 1, l = 3, m = +1, s = +½ |
|
|
B |
n = 3, l = 1, m = +1, s = +½ |
|
|
C |
n = 3, l = 2, m = –3, s = –½ |
|
|
D |
n = 3, l = 2, m = –2, s = –½ |
|
|
E |
n = 3, l = 3, m = –3, s = -½ |
|
|
Pada teori mekanika kuantum, terdapat empat bilangan kuantum yaitu bilangan kuantum utama (n), bilangan kuantum azimuth (l), bilangan kuantum magnetic (m) dan bilangan kuantum spin (s). Berikut ini deretan bilangan kuantum yang tidak mungkin ada dalam atom V dengan nomor atom 23 adalah… |
||
|
A |
n = 1, l = 0, m =0, s = +½ |
|
|
B |
n = 2, l = 0, m =0, s = -½ |
|
|
C |
n = 3, l = 1, m = +1, s = +½ |
|
|
D |
n = 3, l = 2, m = –2, s = +½ |
|
|
E |
n = 4, l = 1, m = –1, s = -½ |
|
|
Kemungkinan harga keempat bilangan kuantum elektron terakhir unsur X adalah n= 3, l =1, m= 0, s = -1/2, maka elektron valensi unsur X adalah… |
||
|
A |
4 |
|
|
B |
5 |
|
|
C |
6 |
|
|
D |
7 |
|
|
E |
8 |
|
|
Pernyataan yang benar terkait dengan sistem periodik Mendeleev adalah…
|
||
|
A |
Jika 1, 2, dan 3 benar |
|
|
B |
jika 1 dan 3 benar |
|
|
C |
jika 2 dan 4 benar |
|
|
D |
jika hanya 4 yang benar |
|
|
E |
jika 1, 2, 3, dan 4 benar |
|
|
Atom Mn dengan konfigurasi elektron: |
||
|
A |
periode 3, golongan VA |
|
|
B |
periode 4, golongan IIA |
|
|
C |
periode 3, golongan VIIB |
|
|
D |
periode 4, golongan VB |
|
|
E |
periode 4, golongan VIIB |
|
|
Suatu atom mempunyai nomor massa 80 dan memiliki jumlah neutron 45. Pada sistem periodic unsur, atom tersebut terletak pada… |
||
|
A |
golongan IA periode 6 |
|
|
B |
golongan IIA periode 6 |
|
|
C |
golongan VIA periode 1 |
|
|
D |
golongan VIA periode 2 |
|
|
E |
golongan VIIA periode 4 |
|
|
Ion |
||
|
A |
golongan IIIB periode 3 |
|
|
B |
golongan VB periode 3 |
|
|
C |
golongan VIIIB periode 4 |
|
|
D |
golongan IA periode 4 |
|
|
E |
golongan IIIA periode 4 |
|
|
Anion |
||
|
A |
golongan VIA periode 4 |
|
|
B |
golongan VIIIA periode 4 |
|
|
C |
golongan IIA periode 5 |
|
|
D |
golongan IIB periode 5 |
|
|
E |
golongan VIIIB periode 4 |
|
|
Pada sistem periodik unsur, suatu unsur berada dalam golongan IIIA periode 4. Unsur tersebut memiliki nomor atom… |
||
|
A |
14 |
|
|
B |
21 |
|
|
C |
22 |
|
|
D |
31 |
|
|
E |
33 |
|
|
Diketahui data nomor atom beberapa unsur sebagai berikut:
Pasangan unsur yang mempunyai kemiripan sifat adalah… |
||
|
A |
P dan Q |
|
|
B |
P dan S |
|
|
C |
Q dan R |
|
|
D |
R dan T |
|
|
E |
S dan T |
|
|
Di antara sifat keperiodikan berikut, sifat yang benar adalah…
|
||
|
A |
Jika 1, 2, dan 3 benar |
|
|
B |
jika 1 dan 3 benar |
|
|
C |
jika 2 dan 4 benar |
|
|
D |
jika hanya 4 yang benar |
|
|
E |
jika 1, 2, 3, dan 4 benar |
|
|
Diberikan beberapa unsur P, Q, R, S, dan T terletak dalam satu periode yang sama pada tabel periodik. Nomor atom unsur-unsur tersebut berturut-turut adalah 13, 14, 15, 16, dan 17. Urutan energi ionisasi yang benar untuk unsur-unsur tersebut, dari yang terkecil hingga terbesar, adalah… |
||
|
A |
P < Q < R < S < T |
|
|
B |
T < S < R < Q < P |
|
|
C |
Q < P < S < R < T |
|
|
D |
P < Q < S < R < T |
|
|
E |
P < R< Q < S < T |
|
|
Jari-jari atom merupakan jarak dari inti atom sampai elektron pada kulit terluar. Di antara atom atau ion di bawah ini yang memiliki jari – jari terbesar adalah… |
||
|
A |
|
|
|
B |
|
|
|
C |
|
|
|
D |
|
|
|
E |
|
|
|
Jika konfigurasi elektron atom unsur:
Pernyataan yang benar adalah… (1) Jari-jari atom A lebih besar dari jari-jari atom B (2) Atom A lebih sukar membentuk ion positif dari pada B (3) Unsur A dan B terletak pada periode yang sama (4) Kelektronegatifan atom A lebih besar dari pada B |
||
|
A |
Jika 1, 2, dan 3 benar |
|
|
B |
Jika 1 dan 3 benar |
|
|
C |
Jika 2 dan 4 benar |
|
|
D |
Jikan hanya 4 yang benar |
|
|
E |
Jika 1, 2, 3, dan 4 benar |
|
|
Jari-jari atom merupakan jarak dari inti atom sampai elektron pada kulit terluar. Diketahui golongan IIA; Be, Mg, Ca, Sr, Ba dengan nomor atom berturut-turut 4, 12, 20, 38, dan 56. Jika diketahui jari-jari atom golongan II A secara acak dalam satuan angstrom adalah 1,05; 2,00; 1,80; 2,15; 1,50. Dari data tersebut yang merupakan jari-jari atom Barium adalah… |
||
|
A |
2,15 |
|
|
B |
1,80 |
|
|
C |
1,05 |
|
|
D |
2,00 |
|
|
E |
1,50 |
|
|
Afinitas elektron merupakan energi yang dilepaskan oleh suatu atom untuk menerima elektron dalam wujud gas. Unsur-unsur berikut yang mempunyai afinitas elektron terbesar adalah… |
||
|
A |
P (Z = 15) |
|
|
B |
Cl (Z = 17) |
|
|
C |
Ar (Z = 18) |
|
|
D |
Ca (Z = 20) |
|
|
E |
Ga (Z = 31) |
|
|
Keelektronegatifan atau elektronegatifan adalah kecenderungan suatu atom dalam menarik pasangan elektron yang digunakan bersama dalam suatu molekul. Pada sistem periodik unsur, unsur-unsur berikut N, O, F, Na, dan Cl dengan nomor atom berturut-turut 7, 8, 9, 11, dan 17 yang memiliki keelektronegatifan paling tinggi adalah… |
||
|
A |
Na |
|
|
B |
N |
|
|
C |
O |
|
|
D |
F |
|
|
E |
Cl |
|
CBT Application
 asam asetat; menggunakan larutan natrium hidroksida;
asam asetat; menggunakan larutan natrium hidroksida;  standar. Untuk melakukan percobaan tersebut, diperlukan alat-alat sebagai berikut :
standar. Untuk melakukan percobaan tersebut, diperlukan alat-alat sebagai berikut :
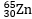
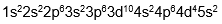
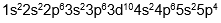
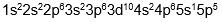
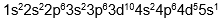
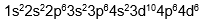
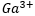 , maka konfigurasi elektron ion
, maka konfigurasi elektron ion 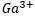 adalah…
adalah…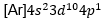
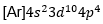
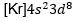
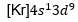
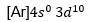
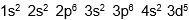 . Dalam sistem periodik unsur, atom Mn terletak pada…
. Dalam sistem periodik unsur, atom Mn terletak pada…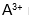
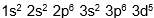 . Pada sistem periodik unsur, atom A terletak pada…
. Pada sistem periodik unsur, atom A terletak pada…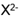 memiliki konfigurasi elektron
memiliki konfigurasi elektron 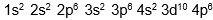 . Pada sistem periodik unsur, atom X terletak pada…
. Pada sistem periodik unsur, atom X terletak pada…